La guerra que libramos contra las bacterias
Lunes,27 mayo 2019En 1947, sólo dos años después de que Fleming recibiese el premio nobel y cuatro desde que se empezase a producir penicilina a gran escala, ya se encontraron bacterias estaphilococcus aureus resistentes a los antibióticos.
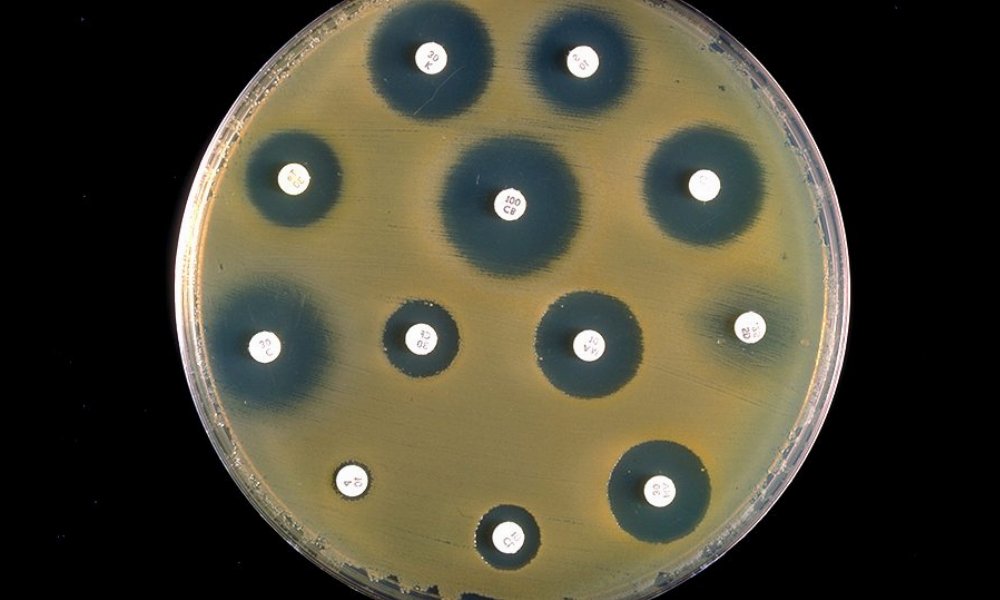
Desde entonces las bacterias han librado su propia guerra cumpliendo su función de supervivencia contra su enemigo a batir: los antibióticos.
Pero hoy conocemos muchas más cosas sobre ellas que antes desconocíamos: evolucionan rapidísimamente (casi nada crece más rápido que las bacterias); tienen un apéndice -pelo ubicado en la superficie de las bacterias- que lo despliegan y absorben así el ADN de las compañeras muertas e incorporan esa información genética, lo que les permite evolucionar hasta convertirse en “superbacterias” (cepas de bacterias resistentes a la mayoría de antibióticos). Esta resistencia se desarrolla de forma natural. Y aun cuando pueda retrasarse, no puede detenerse.
En peligro los avances conseguidos en salud global
Esta resistencia antimicrobiana pone en peligro todos los avances conseguidos en salud global en las últimas décadas. Al tratarse de un fenómeno global y no individual de cada país tiene grandes implicaciones para la salud humana tanto desde el punto de vista de tratamientos de enfermedades infecciosas comunes hasta el freno de los Objetivos de Desarrollo Sostenible (ODS) .
Las cifras
Alrededor de 700.000 muertes al año son debidas en estos momentos a la resistencia a medicamentos. Los expertos consideran que de no cambiar la situación, esta cifra puede llegar a los 10 millones de muertes en el año 2050 y su coste alcanzará los 100 billones de dólares. Según el Banco Mundial, el coste específico en salud para 2050 en el mundo podría variar entre 300.000 millones y más de 1 billón de dólares al año.
La resistencia antimicrobiana puede poner en peligro el éxito de las cirugías mayores y la quimioterapia, que necesitan de antibioterapia para eliminar infecciones secundarias. Otros efectos a destacar son las 480.000 personas que cada año presentan tuberculosis multirresistente o las complicaciones que empiezan a darse en la lucha contra el VIH y la malaria por este motivo.
El nuevo Sistema Mundial de Vigilancia de la Resistencia a los Antimicrobianos de la OMS, denominado GLASS por sus siglas en inglés, ha informado de la presencia generalizada de resistencia a los antibióticos en muestras de 500.000 personas en las que se sospechaban infecciones bacterianas en un estudio en 22 países. En el informe no se contaba con la tuberculosis, que tiene un análisis aparte debido a su enorme relevancia. Las bacterias resistentes más frecuentes eran Escherichia coli, Klebsiella pneumoniae, Staphylococcus aureus y Streptococcus pneumoniae, seguidas de Salmonella. Unas bacterias que están entre las más letales del mundo. La resistencia a la penicilina, el fármaco utilizado durante décadas en todo el mundo para tratar la neumonía osciló entre un 0% y un 51% en los países estudiados. Además, entre un 8% y un 65% de las muestras de E. coli, una bacteria que causa infecciones de las vías urinarias, presentaban resistencia al ciprofloxacino, que es el medicamento que se usa frecuentemente para tratar estas infecciones.
La OMS elaboró en 2017 una lista de patógenos prioritarios para la I+D de nuevos antibióticos con 3 niveles de prioridad, según la resistencia que presentan. En el nivel Según la propia OMS, el 95% del mundo cuenta con planes de acción nacionales para abordar la resistencia antimicrobiana. Pero estos planes aún son muy frágiles en muchos países y necesitan desarrollos tanto a nivel político como técnico de manera urgente. En este sentido la OMS puede proporcionar un apoyo estratégico a los países, pero son éstos quienes deben de considerar la RAM como una prioridad.
La Asamblea Mundial de la Salud de mayo de 2015 adoptó un Plan de acción mundial sobre la resistencia a los antimicrobianos en el que se establecen cinco objetivos:
- Mejorar la concienciación y la comprensión con respecto a la resistencia a los antimicrobianos a través de una comunicación, educación y formación efectivas;
- Reforzar los conocimientos y la base científica a través de la vigilancia y la investigación;
- Reducir la incidencia de las infecciones con medidas eficaces de saneamiento, higiene y prevención de las infecciones;
- Utilizar de forma óptima los medicamentos antimicrobianos en la salud humana y animal;
- Preparar argumentos económicos a favor de una inversión sostenible que tenga en cuenta las necesidades de todos los países, y aumentar la inversión en nuevos medicamentos, medios de diagnóstico, vacunas y otras intervenciones.
Riesgos sanitarios entre las personas, los animales y los ecosistemas
Este Plan Mundial de acción involucra también a la FAO (Organización de las Naciones Unidas para la Alimentación y la Agricultura) y a la OIE (Organización Mundial de Sanidad Animal), porque deben ser parte de la solución a este problema. Para ello han desarrollado el concepto “una sola salud”: la de las personas, los animales, la agricultura y el medio ambiente. En la medicina veterinaria los antibióticos han permitido disminuir el número de infecciones en los animales, algunas de ellas incluso se podían transmitir a las personas. Igualmente los antibióticos han contribuido a la seguridad alimentaria de los cultivos y la inocuidad de alimentos protegiendo la producción agrícola. Pero el abuso de los antibióticos, muchas veces con fines no terapéuticos, sino para promover el crecimiento animal, la venta de medicamentos por internet sin una supervisión sanitaria o el uso de medicamentos falsificados están ayudando a la extensión y gravedad de la RAM. La FAO estima que el consumo de antimicrobianos para animales y cultivos a nivel mundial en el año 2010 fue de 63.151 toneladas. Estos medicamentos se usan sobre todo en la ganadería. La utilización de antimicrobianos en la producción de cultivos es relativamente baja en comparación, situándose entre el 0,2% y el 0,4% del consumo agrícola total.
La resistencia antimicrobiana en los países empobrecidos
Según la FAO, el riesgo de sufrir Resistencia Antimicrobiana parece particularmente alto en los países empobrecidos donde la legislación, los sistemas de vigilancia y seguimiento regulatorios del uso de antimicrobianos, y la prevención y control de la Resistencia a los Antimicrobianos son débiles o insuficientes. El propio Banco Mundial considera la RAM una amenaza para el futuro económico, que podría causar a los países de ingresos bajos una pérdida de más del 5 % del producto interno bruto (PIB) y llevar a 28 millones de personas, la mayoría de países en desarrollo, a la pobreza extrema para 2050. Para la OMS, la gran mayoría de los casos mortales estarían en Asia (4,7 millones) y África (4,1), seguidos de Latinoamérica (392.000), Europa (390.000), Norteamérica (317.000) y Oceanía (22.000).
El uso indebido de los antimicrobianos se ve facilitado en los países pobres por su disponibilidad sin receta, sin prescripción médica a través de cadenas de suministro no reguladas. En 2011, el 100% de los antimicrobianos vendidos en Nigeria y Sudán lo era sin ninguna clase de prescripción médica y en Vietnam alcanzaba el 65%. La fragilidad de los sistemas sanitarios y de regulación de estos países incrementa las posibilidades de unas prácticas de prescripción inapropiadas, y que un gran número de pacientes no cuenten con la información adecuada sobre los medicamentos y la RAM.
Uno de los mayores problemas al tratar de impulsar una estrategia para el uso adecuado de antibióticos tiene que ver con los comportamientos personales de la población. Las informaciones que recibe la población se basan en un discurso biomédico, muchas veces alejado de la realidad del contexto de las poblaciones vulnerables. En estos contextos, donde el dinero no alcanza, es frecuente que no se compren tratamientos completos o se recurra al mercado negro donde predominan los medicamentos falsificados. Y se incrementa el uso de los recursos tradicionales que pueden interaccionar con los tratamientos biomédicos o asistimos a un concepto de enfermedad y salud no exclusivamente biologicista, que puede ver al medicamento con efectos más allá de los puramente biológicos.
Los países en desarrollo se enfrentan a dos retos: (a) mejorar el acceso a los antibióticos necesarios para curar las infecciones que siguen siendo un gran problema de salud para sus poblaciones; (b) la lucha contra la resistencia antimicrobiana, que puede hacer que aunque mejoremos ese acceso a medicamentos no signifique una gran diferencia en cuanto a mortalidad y morbilidad.
Con información de :
La Salud en la Cooperación al Desarrollo y la acción humanitaria. Informe 2018. Cap. 3
Foto antibiograma, de Segundo médico
